Chronische obstructieve longziekte (COPD)
COPD is een veel voorkomende, levensbedreigende longziekte die wereldwijd een van de belangrijkste oorzaken van sterfte en invaliditeit is. Toch is er vaak sprake van onderdiagnose en zijn er nog vele verbeteringen mogelijk in het beheer van deze ziekte.1-3
PART 1
COPD begrijpen
Wat is COPD?
Chronische obstructieve longziekte (COPD) is een veel voorkomende longziekte die leidt tot een beperkte luchtstroom en een steeds sterker bemoeilijkte ademhaling.
Het Global Initiative for Chronic Obstructive Lung Disease (GOLD) definieert COPD als een heterogene longaandoening die wordt gekenmerkt door chronische ademhalingssymptomen als gevolg van afwijkingen van de luchtwegen en/of longblaasjes die aanhoudende, vaak progressieve luchtwegobstructie veroorzaken.3
Belangrijkste symptomen
Symptomen zijn onder meer dyspneu, hoesten en sputumproductie.
Hoewel COPD een chronische ziekte is, krijgt een aanzienlijk aantal patiënten te maken met acute exacerbaties van COPD (een longaanval of AECOPD), die door GOLD worden gedefinieerd als een gebeurtenis die wordt gekenmerkt door een toename van dyspneu en/of hoesten en sputum die in minder dan 14 dagen verergert, die gepaard kan gaan met tachypneu en/of tachycardie en die vaak wordt geassocieerd met toegenomen lokale en systemische ontsteking ten gevolge van infectie, luchtvervuiling of een andere aantasting van de luchtwegen.3
Uit gegevens van verschillende patiëntencohorten blijkt dat tot 70% van de patiënten minstens één longaanval heeft gedurende een follow-up-periode van 1 tot 5 jaar.4
Voor een longaanval is vaak spoedeisende hulp, uitbreiding van de medicatie en/of ziekenhuisopname nodig, wat aanzienlijke extra kosten met zich meebrengt.5
Pathofysiologie
COPD wordt vermoedelijk veroorzaakt door een combinatie van genetische en omgevingsfactoren, met name roken en blootstelling aan luchtvervuiling (beroepsmatige blootstelling en luchtvervuiling binnenshuis door het verbranden van hout en andere biomassabrandstoffen).3
Omdat COPD een heterogene ziekte is, beveelt een panel van specialisten aan om COPD te classificeren op basis van de onderliggende oorzakelijke mechanismen, zodat een gepersonaliseerde behandelingsaanpak kan worden ontwikkeld.2
Ziektelast
COPD veroorzaakt een aanzienlijke economische1 en sociale last.6, 7
COPD beïnvloedt de levenskwaliteit en het geestelijk welzijn van patiënten: COPD wordt geassocieerd met een slechtere lichamelijke gezondheid en ziektespecifieke gezondheidsstatus (vergeleken met mensen zonder COPD)8 en een hoge incidentie van psychiatrische comorbiditeiten9, waaronder depressie.10, 11
COPD is wereldwijd de op 2 na belangrijkste doodsoorzaak en de op 6 na belangrijkste oorzaak van morbiditeit.12
COPD-patiënten lopen het risico regelmatig te worden opgenomen in het ziekenhuis, wat emotioneel zwaar is: bijna 1 op de 5 patiënten die de spoedeisende hulp bezoekt, wordt minstens één keer in het ziekenhuis opgenomen in het jaar na hun eerste bezoek.13
Longaanvallen worden geassocieerd met een afname van de longfunctie14, verslechtering van de levenskwaliteit,15, 16 verminderde lichamelijke activiteit,17 depressie,18 heropnames, verdere longaanvallen en sterfte.19, 20
Comorbiditeiten
Er is sprake van veel comorbiditeiten, vooral cardiovasculaire aandoeningen en diabetes3:
- De meest voorkomende zijn hypertensie, coronaire hartziekte, diabetes, artrose, psychiatrische aandoeningen, astma en obstructief slaapapneusyndroom (OSAS)21, 22
- Comorbiditeiten kunnen de klinische toestand en prognose van een patiënt beïnvloeden en moeten behandeld worden: sommige aandoeningen, zoals hartfalen, ischemische hartziekte, slaapstoornissen en depressie/angst, worden geassocieerd met longaanvallen.3, 23 OSAS kan nachtelijke hypoxemie verergeren en het risico op pulmonale hypertensie verhogen22
Fysieke achteruitgang
De gezondheid van COPD-patiënten vertoont vaak een ‘neerwaartse spiraal’: systemische effecten leiden tot cardiovasculaire comorbiditeiten, spieratrofie en osteoporose, wat resulteert in verdere inactiviteit en fysieke achteruitgang. Evenzo leiden exacerbaties tot een verminderde longfunctie, lichamelijke inactiviteit en een verslechtering van de geestelijke gezondheid.24

COPD begrijpen: samenvatting
COPD is een progressieve longziekte die zich voornamelijk uit door luchtwegobstructie en gepaard gaat met een verminderde levenskwaliteit van de patiënt en een verhoogd risico op overlijden. Hoe vaak komt COPD voor en hoe wordt de diagnose gesteld?
PART 2
Prevalentie en diagnose
Prevalentie
Schattingen van de prevalentie lopen uiteen, maar er wordt aangenomen dat wereldwijd circa 480 miljoen mensen met COPD leven25 en dat de incidentie tussen 1990 en 2019 met >85% is toegenomen.26 De verwachting is dat de incidentie de komende decennia verder zal stijgen door de voortdurende blootstelling aan risicofactoren, een vergrijzende bevolking en een verbeterde bewustwording en diagnose.3
Diagnose
Tekenen en symptomen van COPD kunnen per patiënt en per dag verschillen. Een diagnose moet echter worden overwogen bij elke patiënt die last heeft van aanhoudende dyspneu en chronisch hoesten (met tussenpozen of continu) met of zonder sputumproductie en een voorgeschiedenis van terugkerende infecties van de lagere luchtwegen en/of blootstelling aan risicofactoren zoals roken of luchtvervuiling.3
De beste diagnostische methode is een spirometrietest (de aanwezigheid van een luchtwegbeperking die niet volledig omkeerbaar is met een FEV1/FVC-ratio na bronchodilatatie van <0,7) in combinatie met de klinische voorgeschiedenis en de aanwezigheid van risicofactoren.3
Ondersteunende evaluaties om differentiële diagnoses uit te sluiten, kunnen bestaan uit beeldvorming (röntgenfoto of CT-scan van de borstkas), analyse van arteriële bloedgassen (om hypoxie/hypercapnie op te sporen) en sputumonderzoek (nuttig bij patiënten die een longaanval hebben).3
Diagnose: onvervulde behoeften
Wereldwijd is er sprake van een grote variatie in de gerapporteerde prevalentie van COPD, met onderdiagnose van 10–95% van de patiënten. Dit laatste is vaak het gevolg van onvoldoende of inconsistent gebruik van diagnostische methoden of een gebrekkige beschikbaarheid ervan,27 waarbij sommige patiënten geen toegang hebben tot diagnostische faciliteiten of geschikte gezondheidszorg.
Deskundigen hebben gewezen op diverse zwakke plekken in de huidige diagnostische methoden en criteria. Spirometrie na gebruik van een bronchodilatator is geen voorspeller van symptomen en detecteert vroege pathologische veranderingen niet. Bovendien wordt spirometrie vaak te weinig gebruikt of verkeerd geïnterpreteerd. Een panel van deskundigen geeft aan dat moderne technieken zoals beeldvorming gebruikt zouden kunnen worden om milde COPD op te sporen voordat onomkeerbare pathologische veranderingen zijn opgetreden.2
Classificatie van de ernst
Als leidraad voor de behandelingsaanpak beveelt GOLD aan om COPD in te delen op basis van de mate van luchtwegobstructie (GOLD 1-4) en de symptomen/exacerbatiegeschiedenis3:
- De mate van luchtwegobstructie varieert van mild (GOLD 1) tot zeer ernstig (GOLD 4), afhankelijk van het voorspelde FEV1
- De ernst van de symptomen varieert van GOLD A (weinig symptomen: mMRC 0–1 of CAT<10, geschiedenis van weinig exacerbaties: ≤1 matige exacerbatie) en GOLD B (veel symptomen: mMRC ≥2 of CAT ≥10, geschiedenis van weinig exacerbaties: ≤1 matige exacerbatie) tot GOLD E (elk aantal symptomen, hoog risico op exacerbaties: ≥2 matige exacerbaties of ≥1 exacerbatie resulterend in ziekenhuisopname)

Prevalentie en diagnose: samenvatting
COPD is een heterogene, veel voorkomende longaandoening. Hoewel de symptomen kunnen variëren, is de FEV1/FVC-ratio na gebruik van een bronchodilatator de gouden standaard voor diagnose. Ook de exacerbatiegeschiedenis en symptoomlast worden beoordeeld om de ernst van de ziekte te bepalen. Hoe worden ernstclassificaties gebruikt om de juiste behandeling te kiezen?
PART 3
Behandeling en prognose
Behandeldoelen
De gekozen COPD-behandeling is afhankelijk van de ernst van de ziekte* en heeft als doel om de symptomen te verlichten en tegelijkertijd de ziekteprogressie te vertragen, exacerbaties te verminderen en de mortaliteit te verlagen.
Interventies omvatten veranderingen in levensstijl, farmacologische therapie en zuurstof-/beademingsondersteuning, zoals langdurige zuurstoftherapie en high-flow therapie (Figuur).
*In het GOLD COPD-rapport van 2023 worden drie groepen van symptoomernst erkend – ‘A’, ‘B’ en ‘E’.3
Richtlijnen
De informatie in de volgende onderdelen is niet bedoeld ter vervanging van lokale richtlijnen of aanbevelingen van deskundige organisaties. Raadpleeg de meest recente lokale/internationale richtlijnen om uw behandelbeslissingen op te baseren. Hieronder vindt u enkele relevante links:
https://goldcopd.org/2023-gold-report-2/
Verandering van gedrag/levensstijl
Veranderingen van gedrag en levensstijl omvatten het stoppen met roken en longrevalidatie (lichaamsbeweging in combinatie met patiëntvoorlichting).
Van beide strategieën is aangetoond dat ze de mortaliteit bij patiënten met COPD verlagen.3
Farmacologische behandelingen
Farmacologische behandelingen kunnen de symptomen en de frequentie en ernst van longaanvallen verminderen en de gezondheidstoestand en inspanningstolerantie verbeteren.3
De behandeling moet worden geïndividualiseerd op basis van de ernst van de symptomen, het risico op exacerbaties, bijwerkingen, comorbiditeiten van de patiënt en de beschikbaarheid/kosten van geneesmiddelen, evenals de voorkeuren van de patiënt.3
GOLD beveelt de toediening van bronchodilatatoren via inhalatie aan als centraal onderdeel van de symptoombehandeling. Deze geneesmiddelen helpen gladde luchtwegspieren te ontspannen of hun samentrekking te voorkomen.3
Aan patiënten kunnen antibiotica worden voorgeschreven tijdens een longaanval of ter voorkoming hiervan.28, 29 Patiënten moeten ook worden ingeënt om infecties te voorkomen die tot een longaanval kunnen leiden.3
Mucolytica verminderen het risico op longaanvallen bij sommige patiënten en worden door ERS/ATS aanbevolen voor patiënten met een matige of ernstige luchtwegbeperking en longaanvallen ondanks optimale inhalatietherapie.3, 29
Zuurstoftherapie
O2-therapie kan hypoxemie verlichten en de ademarbeid verminderen. Langdurige O2-therapie moet regelmatig opnieuw worden geëvalueerd en wordt door GOLD en ATS aanbevolen voor patiënten met ernstige hypoxemie in rust, bij wie dit gepaard gaat met een kleine toename in overleving.3, 30, 31
O2 kan worden toegediend door middel van een zuurstofconcentrator, een cilinder met gecomprimeerde of vloeibare zuurstof of via een beademingsapparaat.
High-flow therapie (HFT)
HFT levert een bevochtigd, verwarmd luchtmengsel met of zonder O2 en kan patiënten helpen die last hebben van chronische hoest en slijmproductie, symptomen die soms moeilijk te behandelen zijn met alleen standaardtherapieën.32
HFT is ontworpen om te worden toegediend via een high-flow neuscanule (NHFC). Thuis-HFT kan een flow leveren van 10-60 l/min of van 10-15 l/min indien O2 wordt toegevoegd. De gebruikte configuratie hangt af van de behoeften van de patiënt.
Tot de voordelen van HFT behoren verbeterd secretiebehee,33 minder dyspneu,34-36 een kleinere dode ruimte,37 meer comfort voor de patiënt33, 37 en minder longaanvallen.32, 38
Non-invasieve beademing (NIV) in de thuisomgeving
NIV wordt door GOLD en ERS aanbevolen voor stabiele patiënten met ernstige chronische hypercapnie en een voorgeschiedenis van ziekenhuisopname wegens acuut respiratoir falen.3, 39-41
- Voordelen zijn onder meer een betere overleving en levenskwaliteit en een verlaagd risico op ziekenhuisopname39, 40
- Er is aangetoond dat NIV in combinatie met O2-therapie in de thuisomgeving na een longaanval de tijd tot heropname of overlijden aanzienlijk verlengt, resulteert in minder nieuwe longaanvallen40 en kosteneffectief is42
- Gegevens uit klinisch onderzoek onderstrepen het belang van een zorgvuldige evaluatie van het fenotype van de patiënt en van de timing en toediening van thuis-NIV om te verzekeren dat patiënten worden geselecteerd die er waarschijnlijk het meeste baat bij hebben43
Beste praktijken voor thuis-NIV
Overwegingen voor beste praktijken voor thuis-NIV omvatten de zorgvuldige selectie van patiënten die het meest waarschijnlijk baat zullen hebben bij de behandeling, het geven van een therapie die effectief is en goed wordt verdragen en het zorgvuldig opvolgen van de effecten van de behandeling.
Het verlagen van verhoogde arteriële kooldioxideconcentraties dient een van de belangrijkste doelen van thuis-NIV te zijn en gegevens uit klinisch onderzoek tonen aan dat een hogere inspiratoire druk bijdraagt aan het succes van NIV-therapie in de thuisomgeving.39, 40, 44
NIV voor acute voorvallen
GOLD beveelt NIV ook aan voor de behandeling van longaanvallen wanneer er sprake is van respiratoire acidose / ernstige dyspneu waarbij er klinische aanwijzingen zijn voor vermoeidheid van de ademhalingsspieren / aanhoudende hypoxemie ondanks aanvullende O2.3
ERS en ATS bevelen NIV aan voor acuut-bij-chronisch hypercapnisch respiratoir falen als gevolg van een longaanval.28
Kosteneffectiviteit van thuis starten met NIV in plaats van in het ziekenhuis
Keuze uit LTOT, HFT of NIV
LTOT, thuis-HFT en thuis-NIV kunnen afzonderlijk of in combinatie worden gebruikt voor de behandeling van COPD-patiënten in de thuisomgeving. Enkele voordelen van elke benadering worden weergegeven in de tabel.
CPAP (continuous positive airway pressure)
Sommige patiënten kunnen ook baat hebben bij CPAP, waarvan is aangetoond dat het de overleving verbetert en het risico op ziekenhuisopname vermindert bij patiënten met zowel COPD als obstructief slaapapneusyndroom.3
Chirurgie
Chirurgische opties zijn longvolumereductie, bullectomie en longtransplantatie.
Prognose
Hoewel COPD een progressieve ziekte is, kan een geschikte behandeling de symptomen en de frequentie en ernst van exacerbaties verminderen en de gezondheidstoestand en inspanningstolerantie verbeteren.3
Sommige behandelingen kunnen ook de achteruitgang van de longfunctie vertragen en de mortaliteit verlagen.3
Er is aangetoond dat langdurige O2-therapie de overleving verbetert van patiënten met ernstige hypoxemie in rust en NIV verlaagt de mortaliteit en voorkomt heropname in het ziekenhuis bij patiënten met ernstige chronische hypercapnie.3
Onbehandelde COPD kan leiden tot acuut of chronisch respiratoir falen. Patiënten lopen vooral risico tijdens een longaanval, omdat bij een toename van de luchtwegobstructie het ademhalingsstelsel snel overbelast kan raken.
Toekomstperspectief
Er is dringend behoefte aan een sterkere aanpak van COPD op wereldwijd niveau.46
Een panel van deskundigen merkt in een artikel in The Lancet op dat een gecoördineerde internationale respons (zoals bij COVID-19) bestaande barrières voor behandeling kan overwinnen en snelle resultaten kan opleveren. In het bijzonder pleiten zij voor2:
- Volksgezondheidsstrategieën om roken te verbieden en de lucht schoon te houden
- Een gepersonaliseerde medische aanpak – gebaseerd op een uitgebreide beoordeling van de pathofysiologie en symptomen van de ziekte, evenals de behoeften, mogelijkheden en voorkeuren van de patiënten
- Meer investeringen in curatieve en regeneratieve therapieën om meer te kunnen bieden dan grotendeels symptomatische behandelingsopties
- Grotere aandacht voor longaanvallen, die een cruciale rol spelen bij de ziekteprogressie en kosten, maar vaak onnauwkeurig gedefinieerd en onvoldoende onderzocht worden.
Lees de infographics om meer te weten te komen over enkele van de belangrijkste onvervulde behoeften in de zorg voor COPD;

Behandeling en prognose: samenvatting
COPD is een progressieve ziekte die de levenskwaliteit van patiënten aanzienlijk beïnvloedt en wereldwijd een belangrijke oorzaak is van morbiditeit en mortaliteit.3, 6, 12 Het is echter aangetoond dat adequate behandeling de symptomen, de frequentie en ernst van longaanvallen,3, 32 en, bij patiënten met COPD en chronische hypercapnie die worden behandeld met non-invasieve beademing, de overleving kan verbeteren.39
Deze inhoud is uitsluitend bestemd voor zorgprofessionals.
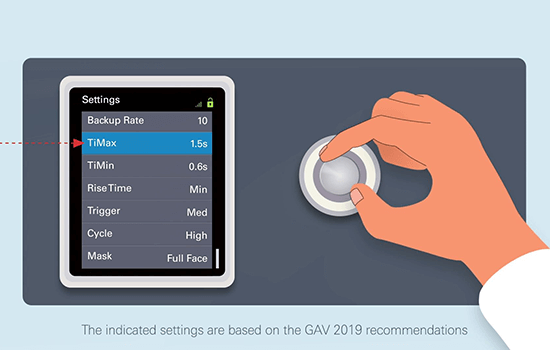
**Deze instructievideo’s over het gebruik van thuis-NIV zijn alleen bedoeld voor zorgprofessionals en zijn gebaseerd op de GAV-aanbevelingen van 2019, die zelf weer gebaseerd zijn op de literatuur en de input van ervaren ademhalingstherapeuten. Het zorgprotocol blijft de verantwoordelijkheid van de voorschrijvende arts en de apparaatinstellingen moeten worden gekozen op basis van de behoeften van elke patiënt.
Referenties
- Iheanacho, I., et al., Economic Burden of Chronic Obstructive Pulmonary Disease (COPD): A Systematic Literature Review. Int J Chron Obstruct Pulmon Dis, 2020. 15: p. 439-460.
- Stolz, D., et al., Towards the elimination of chronic obstructive pulmonary disease: a Lancet Commission. Lancet, 2022. 400(10356): p. 921-972.
- Global Initiative for Chronic Obstructive Lung Disease. Global Strategy for the Prevention, Diagnosis and Management of COPD: 2023 Report 2023. Available at https://goldcopd.org/2023-gold-report-2/
- Hoogendoorn, M., et al., Prediction models for exacerbations in different COPD patient populations: comparing results of five large data sources. Int J Chron Obstruct Pulmon Dis, 2017. 12: p. 3183-3194.
- Dalal, A.A., et al., Impact of COPD Exacerbation Frequency on Costs for a Managed Care Population. J Manag Care Spec Pharm, 2015. 21(7): p. 575-83.
- Svedsater, H., et al., Life Impact and Treatment Preferences of Individuals with Asthma and Chronic Obstructive Pulmonary Disease: Results from Qualitative Interviews and Focus Groups. Adv Ther, 2017. 34(6): p. 1466-1481.
- Cook, N.S., et al., Patients’ perspectives on COPD: findings from a social media listening study. ERJ Open Res, 2019. 5(1).
- Franssen, F.M.E., et al., The physical, mental, and social impact of COPD in a population-based sample: results from the Longitudinal Aging Study Amsterdam. NPJ Prim Care Respir Med, 2018. 28(1): p. 30.
- FitzGerald, J.M., et al., Resource use study in COPD (RUSIC): a prospective study to quantify the effects of COPD exacerbations on health care resource use among COPD patients. Can Respir J, 2007. 14(3): p. 145-52.
- Omachi, T.A., et al., Depression and health-related quality of life in chronic obstructive pulmonary disease. Am J Med, 2009. 122(8): p. 778 e9-15.
- Zhang, M.W., et al., Prevalence of depressive symptoms in patients with chronic obstructive pulmonary disease: a systematic review, meta-analysis and meta-regression. Gen Hosp Psychiatry, 2011. 33(3): p. 217-23.
- GBD 2019 Diseases and Injuries Collaborators, Global burden of 369 diseases and injuries in 204 countries and territories, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019. Lancet, 2020. 396(10258): p. 1204-1222.
- Yeatts, K.B., et al., Population-based burden of COPD-related visits in the ED: return ED visits, hospital admissions, and comorbidity risks. Chest, 2013. 144(3): p. 784-793.
- Donaldson, G.C., et al., Relationship between exacerbation frequency and lung function decline in chronic obstructive pulmonary disease. Thorax, 2002. 57(10): p. 847-52.
- Miravitlles, M., et al., Effect of exacerbations on quality of life in patients with chronic obstructive pulmonary disease: a 2 year follow up study. Thorax, 2004. 59(5): p. 387-95.
- Seemungal, T.A., et al., Effect of exacerbation on quality of life in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med, 1998. 157(5 Pt 1): p. 1418-22.
- Ehsan, M., et al., A longitudinal study evaluating the effect of exacerbations on physical activity in patients with chronic obstructive pulmonary disease. Ann Am Thorac Soc, 2013. 10(6): p. 559-64.
- Alahmari, A.D., et al., Physical activity and exercise capacity in patients with moderate COPD exacerbations. Eur Respir J, 2016. 48(2): p. 340-9.
- Suissa, S., S. Dell’Aniello, and P. Ernst, Long-term natural history of chronic obstructive pulmonary disease: severe exacerbations and mortality. Thorax, 2012. 67(11): p. 957-63.
- Connors, A.F., Jr., et al., Outcomes following acute exacerbation of severe chronic obstructive lung disease. The SUPPORT investigators (Study to Understand Prognoses and Preferences for Outcomes and Risks of Treatments). Am J Respir Crit Care Med, 1996. 154(4 Pt 1): p. 959-67.
- Santos, N.C.D., et al., Prevalence and Impact of Comorbidities in Individuals with Chronic Obstructive Pulmonary Disease: A Systematic Review. Tuberc Respir Dis (Seoul), 2022. 85(3): p. 205-220.
- Soler, X., et al., High Prevalence of Obstructive Sleep Apnea in Patients with Moderate to Severe Chronic Obstructive Pulmonary Disease. Ann Am Thorac Soc, 2015. 12(8): p. 1219-25.
- Stallberg, B., et al., Real-world retrospective cohort study ARCTIC shows burden of comorbidities in Swedish COPD versus non-COPD patients. NPJ Prim Care Respir Med, 2018. 28(1): p. 33.
- Hurst, J.R., et al., Understanding the impact of chronic obstructive pulmonary disease exacerbations on patient health and quality of life. Eur J Intern Med, 2020. 73: p. 1-6.
- Boers, E., et al. An estimate of the global COPD prevalence in 2050: Disparities by income and gender. Poster presented at the European Respiratory Society International Congress 2022. Barcelona, Spain.
- Li, H.Y., et al., Global, regional and national burden of chronic obstructive pulmonary disease over a 30-year period: Estimates from the 1990 to 2019 Global Burden of Disease Study. Respirology, 2023. 28(1): p. 29-36.
- Ho, T., et al., Under- and over-diagnosis of COPD: a global perspective. Breathe (Sheff), 2019. 15(1): p. 24-35.
- Wedzicha, J.A.E.C.-C., et al., Management of COPD exacerbations: a European Respiratory Society/American Thoracic Society guideline. Eur Respir J, 2017. 49(3).
- Wedzicha, J.A., et al., Prevention of COPD exacerbations: a European Respiratory Society/American Thoracic Society guideline. Eur Respir J, 2017. 50(3).
- Jacobs, S.S., et al., Home Oxygen Therapy for Adults with Chronic Lung Disease. An Official American Thoracic Society Clinical Practice Guideline. Am J Respir Crit Care Med, 2020. 202(10): p. e121-e141.
- Cranston, J.M., et al., Domiciliary oxygen for chronic obstructive pulmonary disease. Cochrane Database Syst Rev, 2005. 2005(4): p. CD001744.
- Storgaard, L.H., et al., Long-term effects of oxygen-enriched high-flow nasal cannula treatment in COPD patients with chronic hypoxemic respiratory failure. Int J Chron Obstruct Pulmon Dis, 2018. 13: p. 1195-1205.
- Hasani, A., et al., Domiciliary humidification improves lung mucociliary clearance in patients with bronchiectasis. Chron Respir Dis, 2008. 5(2): p. 81-6.
- Cirio, S., et al., Effects of heated and humidified high flow gases during high-intensity constant-load exercise on severe COPD patients with ventilatory limitation. Respir Med, 2016. 118: p. 128-132.
- Neunhauserer, D., et al., Supplemental Oxygen During High-Intensity Exercise Training in Nonhypoxemic Chronic Obstructive Pulmonary Disease. Am J Med, 2016. 129(11): p. 1185-1193.
- Chatila, W., et al., The effects of high-flow vs low-flow oxygen on exercise in advanced obstructive airways disease. Chest, 2004. 126(4): p. 1108-15.
- Fraser, J.F., et al., Nasal high flow oxygen therapy in patients with COPD reduces respiratory rate and tissue carbon dioxide while increasing tidal and end-expiratory lung volumes: a randomised crossover trial. Thorax, 2016. 71(8): p. 759-61.
- Rea, H., et al., The clinical utility of long-term humidification therapy in chronic airway disease. Respir Med, 2010. 104(4): p. 525-33.
- Kohnlein, T., et al., Non-invasive positive pressure ventilation for the treatment of severe stable chronic obstructive pulmonary disease: a prospective, multicentre, randomised, controlled clinical trial. Lancet Respir Med, 2014. 2(9): p. 698-705.
- Murphy, P.B., et al., Effect of Home Noninvasive Ventilation With Oxygen Therapy vs Oxygen Therapy Alone on Hospital Readmission or Death After an Acute COPD Exacerbation: A Randomized Clinical Trial. JAMA, 2017. 317(21): p. 2177-2186.
- Ergan, B., et al., European Respiratory Society guidelines on long-term home non-invasive ventilation for management of COPD. Eur Respir J, 2019. 54(3).
- Murphy, P.B., et al., Cost-effectiveness of home non-invasive ventilation in patients with persistent hypercapnia after an acute exacerbation of COPD in the UK. Thorax, 2023. 78(5): p. 523-525.
- Murphy, P.B. and N. Hart, Home Non-Invasive Ventilation for COPD: How, Who and When? Arch Bronconeumol (Engl Ed), 2018. 54(3): p. 149-154.
- Windisch, W., J.H. Storre, and T. Kohnlein, Nocturnal non-invasive positive pressure ventilation for COPD. Expert Rev Respir Med, 2015. 9(3): p. 295-308.
- Duiverman, M.L., et al., Home initiation of chronic non-invasive ventilation in COPD patients with chronic hypercapnic respiratory failure: a randomised controlled trial. Thorax, 2020. 75(3): p. 244-252.
- Halpin, D.M.G., et al., It is time for the world to take COPD seriously: a statement from the GOLD board of directors.Eur Respir J, 2019. 54(1).